
Kinderwunsch
FRUCHTBARKEITS-
RESERVEN
KRYOKONSERVIERUNG VON UNBEFRUCHTETEN EIZELLEN/ ANLEGEN EINER FRUCHTBARKEITSRESERVE
Der Wunsch nach eigenen Kindern ist für viele Menschen zentral in ihrer Lebensplanung. Verschiedene Gründe, wie berufliche oder persönliche Umstände, können dazu führen, die Familiengründung aufzuschieben. Das Einfrieren unbefruchteter Eizellen als Fruchtbarkeitsreserve ermöglicht es, eine Schwangerschaft auch später noch zu realisieren. Bei Krebserkrankungen kann das schnelle Einfrieren von Eizellen vor einer Chemotherapie wichtig sein. Hat die Frau einen Partner, können bereits befruchtete Eizellen gesichert werden. Auch ohne medizinischen Grund, etwa aus persönlichen Überlegungen („social-freezing“), entscheiden sich manche Frauen für das Anlegen einer Eizellreserve.
ABLAUF
DER KRYOKONSERVIERUNG VON EIZELLEN
FÖRDERUNG DER EIZELLREIFUNG (STIMULATION)
Um genügend Eizellen für die Kryokonservierung zu gewinnen, erfolgt zunächst eine hormonelle Stimulation, die das gleichzeitige Heranreifen mehrerer Eibläschen bewirkt. Während dieser Phase kontrollieren wir den Reifezustand regelmäßig per Ultraschall und bestimmen bei Bedarf per Blutuntersuchung den optimalen Zeitpunkt für das Auslösen des Eisprung und die Entnahme befruchtungsfähiger Eizellen.
AUSLÖSEN DES EISPRUNGS UND ENTNAHME DER EIZELLEN
Sobald die Eizellen das optimale Reifestadium erreicht haben, wird der Eisprung durch eine Spritze (z. B. hCG-Injektion) ausgelöst. Dadurch löst sich die Eizelle von der Follikel-Innenwand und kann dann durch eine Punktion aus dem Eierstock entnommen werden. Nicht jedes Eibläschen enthält eine Eizelle, so dass die Anzahl der im Ultraschall sichtbaren Follikel in der Regel höher ist, als die Anzahl der gewonnenen Ezellen.

KRYOKONSERVIERUNG DER EIZELLEN
Nach der Entnahme werden die Eizellen mikroskopisch geprüft und durch „ultraschnelles Einfrieren“ (Vitrifikation) bei -196 °C in flüssigem Stickstoff konserviert. Die Proben werden sicher im Depot der Firma Air-Liquid in Krefeld gelagert. Laut aktuellem Wissensstand ist eine jahrelange Lagerung möglich, ohne das Risiko für das zukünftige Kind zu erhöhen.

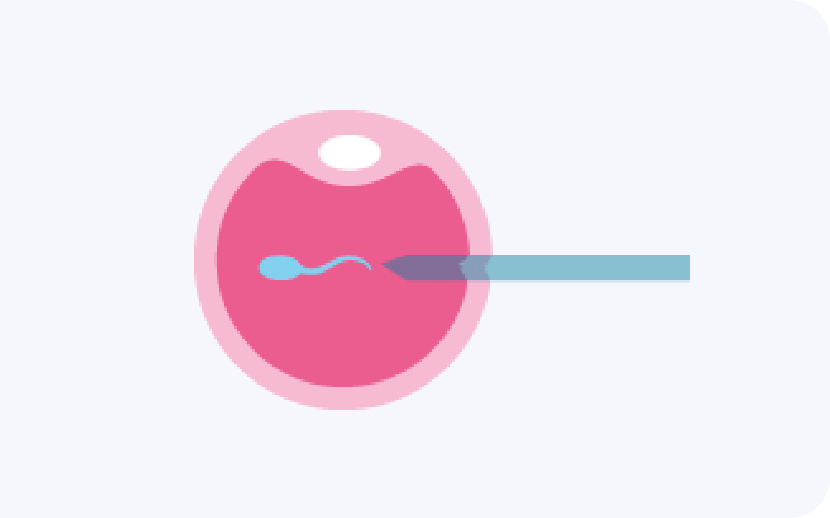
AUFTAUVORGANG UND BEFRUCHTUNG DER EIZELLEN
Auf Wunsch der Patientin/des Paares werden die eingefrorenen Eizellen bzw. Vorkernstadien zu einem späteren Zeitpunkt in unser Zentrum überführt. Die Eizellen werden anschließend aufgetaut und mit den Samenzellen des Mannes befruchtet. Die Befruchtung kryokonservierter Eizellen erfolgt durch die ICSI-Methode (intracytoplasmatische Spermiuminjektion).
ABLAUF
DER KRYOKONSERVIERUNG VON SPERMIEN
Der Wunsch nach eigenen Kindern ist für viele zentral in der Lebensplanung. Die Fruchtbarkeit des Mannes nimmt mit dem Alter ab, und bestimmte Erkrankungen können die Zeugungsfähigkeit beeinträchtigen. Die Kryokonservierung von Spermien ist hier eine bewährte Methode, etwa bei:
– Krebserkrankungen, Chemotherapie oder Bestrahlung, die die Spermienproduktion beeinträchtigen können
– Stark eingeschränkter Samenqualität, die sich voraussichtlich weiter verschlechtert
– Geplanter Sterilisation Betroffenen Männern wird empfohlen, eine oder mehrere Samenproben einzufrieren, um den Kinderwunsch später noch erfüllen zu können.
GEWINNUNG
Die Samenprobe wird vor der Kryokonservierung durch Masturbation gewonnen. Unser Spenderaum bietet dafür Ruhe und Diskretion. Alternativ kann die Probe von zu Hause mitgebracht werden, jedoch nur in einem speziellen Probenbecher und durch persönliche Übergabe. Dabei sind die Empfehlungen zur Sperma-Gewinnung zu beachten, und ein vorheriger Test auf Hepatitis und HIV ist erforderlich. Nach Untersuchung der Probe entscheiden wir, ob die Anzahl und Beweglichkeit der Spermien für eine Kryokonservierung ausreichen.

KRYOKONSERVIERUNG
Bei ausreichender Qualität wird die Samenprobe mit einem Gefrierschutzmedium gemischt, in mehreren Halmen eingefroren und solange gelagert, bis der Kinderwunsch realisiert werden soll. Die Lagerung erfolgt bei -196 C in flüssigem Stickstoff. Ist eine Verwendung der Spermien erst in fernerer Zukunft vorgesehen, werden diese in das Depot der Firma Air-Liquid in Krefeld überführt und dort sicher gelagert. Nach momentanem Stand der Wissenschaft, kann die Lagerung der Spermien für viele Jahre erfolgen, ohne dass hieraus ein erhöhtes Risiko für das zu zeugende Kind entsteht.

Vor Therapiebeginn findet ein Beratungsgespräch statt, um die individuelle Situation und Behandlung zu besprechen. Die Eizellqualität und damit der Erfolg der Kryokonservierung hängen stark vom Alter ab; daher wird das Einfrieren vor dem 35. Lebensjahr empfohlen. Die Überlebensrate der aufgetauten Eizellen liegt derzeit bei 80-90 %, die Befruchtungsrate bei 60-70 %. Da nicht jeder Embryo sich einnistet, streben wir an, mindestens 20 Eizellen einzufrieren, was oft zwei Stimulationszyklen erfordert – bei Frauen unter 25 Jahren manchmal nur einen. Die Rückübertragung der Eizellen ist bis zum 45. Lebensjahr möglich, da spätere Schwangerschaften medizinisch und sozial als nicht verantwortbar gelten.
ABLAUF
DER KRYOKONSERVIERUNG VON HODENGEWEBE
Neben dem Einfrieren ejakulierter Spermien, besteht die Möglichkeit der Kryokonservierung von Hodengewebe, welches im Rahmen einer TESE (testikuläre Spermienextraktion) gewonnen wurde. Aus diesem Gewebe können oft in einem weiteren Schritt Spermien gewonnen werden, die dann im Rahmen einer ICSI-Therapie zur Befruchtung von Eizellen verwendet werden. Die Einlagerung von Hodengewebe kommt z.B. bei Patienten mit einem Verschluss des Samenleiters zum Einsatz. Gründe für einen solchen Verschluss können z.B. eine vorangegangene Sterilisation oder auch eine genetische Erkrankung sein.

